1.
推理是一种重要的思维方法,以下推理合理的是( )
A.
因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件
B.
铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀
C.
因为O3和O2的组成元素相同,所以两者的化学性质完全相同
D.
碱性溶液的pH都大于7,所以碱溶液pH一定大于7
【考点】
溶液的酸碱性与pH值的关系;
金属的化学性质;







 在一定量AgNO3和Zn(NO3)2的混合溶液中加入铁粉
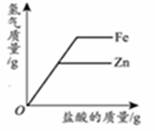
在一定量AgNO3和Zn(NO3)2的混合溶液中加入铁粉 向等质量的锌粉和铁粉中,分别加入相同质量分数的稀盐酸
向等质量的锌粉和铁粉中,分别加入相同质量分数的稀盐酸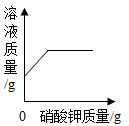 常温下,向硝酸钾的不饱和溶液中加入硝酸钾晶体
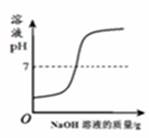
常温下,向硝酸钾的不饱和溶液中加入硝酸钾晶体 向一定量的稀盐酸中加入过量的NaOH溶液
向一定量的稀盐酸中加入过量的NaOH溶液