1.
某兴趣小组做了如下实验:
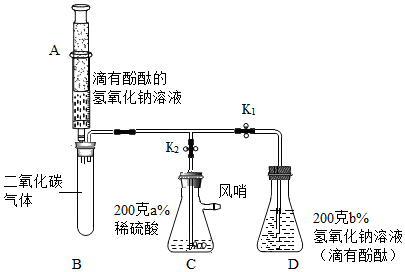
①在止水夹K1、K2处于关闭状态时,将针筒A中溶液挤入试管B中,接着打开止水夹K1 , 发现D中的部分溶液被吸入试管B中,充分反应后,试管B留下的溶液也显红色;
②打开止水夹K2 , 风哨振动鸣叫,C中的部分溶液被吸入B和D中,反应后B、D中溶液都变为无色。
回答:
(1)
步骤①中,充分反应后,试管B里的CO2最终转化为(填化学式)和水。
(2)
解释步骤②中“风哨振动鸣叫”的原因。
(3)
实验开始时C、D中两种溶液中溶质质量分数大小关系为:a%b%(选填“>”“=”“<”)
【考点】
酸的化学性质;
碱的化学性质;
能力提升
真题演练

