1.
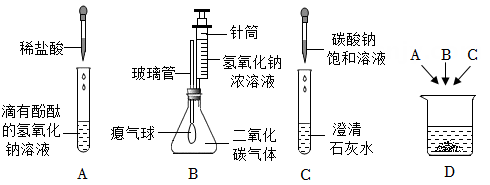
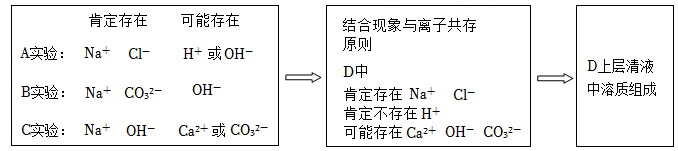
小越在做“碱和盐的性质”实验时,将氢氧化钠溶液加入氯化钙溶液中,观察到有白色沉淀产生。白色沉淀是怎么产生的呢?
小陈认为是氢氧化钠溶液变质产生的碳酸钠与氯化钙溶液反应,生成了碳酸钙沉淀。小越猜想:除了这种可能性外,还可能是氢氧化钠与氯化钙交换成分,生成氢氧化钙和氯化钠,由于氢氧化钙溶解度较小,从溶液中析出,产生白色沉淀。
为了检验小越的猜想,小陈设计了如下实验:
取小越实验所用的氢氧化钠溶液,加入过量的氯化钡溶液,静置后取上层液体加入氯化钙溶液,产生了白色沉淀。取该白色沉淀少许,加水后沉淀溶解,再向其中通入二氧化碳气体,观察到产生白色沉淀。
(1)
久置的氢氧化钠溶液变质的原因是(用化学方程式表示);
(2)
小陈在氢氧化钠溶液中加入过量的氯化钡溶液的目的是;
(3)
小越的猜想经检验是(选填“正确”或“错误”)的。
【考点】
实验方案设计与评价;
碱的化学性质;
能力提升
真题演练