1.
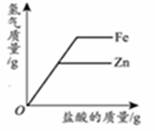
金属与酸的置换反应:
Fe+2HCl=
Zn+H2SO4= (实验室制H2)
只有排在金属活动性顺序 的金属才能和酸发生置换反应。
【考点】
金属的化学性质;
金属活动性顺序及其应用;
基础巩固
能力提升
变式训练
拓展培优
真题演练