1.
小明对金属活动性顺序等知识进行了研究。

(1)
将甲、乙两种金属片分别放入硫酸铜溶液中,乙表面析出红色固体,甲没有明显现象。判断甲、乙、铜三种金属的活动性由强到弱的顺序为。
(2)
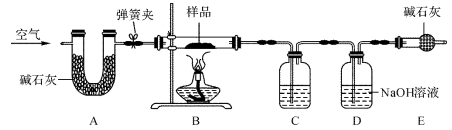
查阅资料:在金属活动性顺序里,位于氢后面的金属Cu,在常温下虽然不能与稀盐酸、稀硫酸反应,但可以与稀硝酸反应,其化学方程式为:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。反应生成的NO是无色、难溶于水的气体,在常温下与空气中的O2迅速化合生成NO2 , NO2是红棕色、有刺激性气味的有毒气体。用下图所示实验装置进行实验,可以证明铜与稀硝酸反应生成的气体是NO。
①检查装置的气密性:关闭弹簧夹,将干燥管放入带有水的烧杯中,若观察到,则表明该装置的气密性良好。
②按上图所示进行实验:打开弹簧夹,用注射器慢慢抽取干燥管内的气体,稀硝酸沿着干燥管慢慢上升,直到,停止抽拉注射器,关闭弹簧夹,观察干燥管内的现象:。反应停止后,打开弹簧夹,用注射器抽取干燥管内的气体(事先已将注射器内原有的气体推出),关闭弹簧夹后取下注射器,并抽取一定量的空气,观察到气体变为红棕色。
③述实验完成后,将注射器内的气体压入足量NaOH溶液中,其目的是。
④在3.84gCu中加入100g稀HNO3溶液,如恰好完全反应,计算生成NO的质量为。
【考点】
实验方案设计与评价;
常见实验操作;
根据化学反应方程式的计算;
金属活动性顺序及其应用;
能力提升