1.
同学们分别设计了如图所示的三个实验用于验证质量守恒定律。

(1)
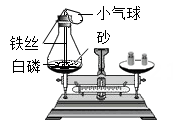
实验甲:首先称量锥形瓶装置的质量,然后点燃白磷,待反应完毕装置冷却后再次称量,天平仍然平衡。实验中标志着化学反应发生的现象是,小气球的作用是。用加热的玻璃管点燃白磷时,若瓶塞未塞紧,待燃烧完毕后再塞紧,天平的指针将会(填“偏左”“偏右”或“正中”)。
(2)
实验乙:反应前天平平衡,然后将稀盐酸倒入烧杯中与石灰石充分反应后再称量,观察到反应后天平不平衡,天平指针向右偏转,其原因是。
(3)
实验丙:在一根用细铜丝吊着的长玻璃棒两端分别绕上10厘米长的粗铜线,并使玻璃棒保持水平。然后用酒精灯给左边一端铜丝加热1~2分钟。冷却后,观察到的现象:①;②。其原因用化学方程式表示为。
(4)
反思总结:在三个实验中,是否有不遵循质量守恒定律的反应?。设计实验验证质量守恒定律,当选用有气体参加或生成的化学反应时,要注意;从原子的角度解释质量守恒的原因是。
【考点】
质量守恒定律及其应用;
能力提升
真题演练