1.
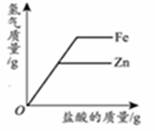
人类对科学规律的认识常需经历漫长的探索过程,对金属活动性规律的认识也是如此。小金运用该规律开展实验,向硝酸铜和硝酸银的混合溶液中逐渐加入铁粉,溶液质量变化如图所示。

(1)B点时溶液中所含的金属阳离子有。
(2)C点之后,溶液中存在的金属为。
【考点】
金属的化学性质;
金属活动性顺序及其应用;
基础巩固
能力提升
变式训练
拓展培优
真题演练