1.
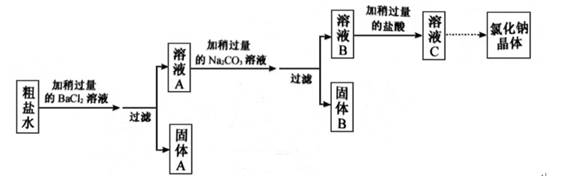
氯碱工业以粗盐(主要成分是NaCl,含少量泥沙、 、
、 )为原料,生产氯气和氢氧化钠,模拟流程如图:
)为原料,生产氯气和氢氧化钠,模拟流程如图:

(1)
试剂A与试剂B的组合为(填序号)。
(2)
操作A需使用玻璃棒,玻璃棒的作用是。
(3)
流程中Mg元素必须转化成(填化学式)才能完全除去。
(4)
该工业副产品 , 氢能是未来最理想的能源,从环保角度分析,氢能最突出的优点是。氢氧燃料电池已经被应用,氢氧燃料电池是一种将化学能转化为能的装置。目前还不能作为燃料被广泛应用,其理由(答一条即可)。
, 氢能是未来最理想的能源,从环保角度分析,氢能最突出的优点是。氢氧燃料电池已经被应用,氢氧燃料电池是一种将化学能转化为能的装置。目前还不能作为燃料被广泛应用,其理由(答一条即可)。
①KOH ②NaOH ③ ④
【考点】
蒸发操作与粗盐提纯;
盐的性质及用途;
能力提升
真题演练